Blogger: Sofie Snipstad, stipendiat ved Institutt for fysikk, og vinner av årets Forsker Grand Prix!
Hun samarbeider blant annet med Institutt for laboratoriemedisin, barn- og kvinnesykdommer og Institutt for kreftforskning og molekylær medisin ved Det medisinske fakultet, og Avdeling for patologi og medisinsk genetikk og Kreftklinikken ved St. Olavs Hospital.
Kreft oppstår når en celle i kroppen blir skadet, begynner å dele seg ukontrollert, og danner en svulst. I Norge får hver tredje person kreft i løpet av livet, bare i 2015 ble det registrert over 32 000 nye tilfeller. Heldigvis viser tallene også at overlevelsen øker, fordi vi oppdager kreft tidligere og fordi behandlingen blir bedre, men prisen for å ta medisin kan være høy.
En vanlig del av dagens kreftbehandling er cellegift, enten alene eller i kombinasjon med stråling eller operasjon. Problemet er at cellegiften sprer seg til hele kroppen og skader de friske cellene våre. Dette fører til en rekke bivirkninger, som i noen tilfeller blir så alvorlige at behandlingen må avsluttes. En annen utfordring er at når alle cellene i kroppen deler på medisinen, så er det veldig lite som ender opp der egentlig vil ha den, så lite som 0.01 % av dosen når frem til svulsten. Jeg jobber derfor med å levere mer cellegift til svulsten, og mindre til resten av kroppen. Hvis vi får til det kan vi redusere dosen cellegift som pasienten får, få færre bivirkninger av behandlingen, men likevel god effekt av medisinen. Det vi gjør er å kapsle cellegiften inn i nanopartikler.
Kan nanomedisin hjelpe?
Disse nanopartiklene kan sprøytes inn i blodet. I motsetning til cellegiften, er nanopartiklene så store at de ikke slipper ut av blodårene i de fleste typer friskt vev. I svulsten derimot, har blodårene porøse vegger slik at nanopartiklene slipper ut. På den måten har vi et målsøkende transportmiddel som frakter medisinen til de syke cellene. Jeg har vist at vi på denne måten kan få levert hele 100 ganger mer av dosen til svulsten, sammenlignet med bruk av tradisjonell cellegift alene. Dette er veldig interessant, og det finnes allerede noen få nanomedisiner som er godkjente for bruk i klinikken.
Men nanopartiklene når bare fram til de cellene som er nærmest blodåren, og cellene som er langt unna blir dermed ikke påvirket. I tillegg har det vist seg at det er store variasjoner mellom ulike svulster og innad i svulster på hvor lekke disse blodårene faktisk er. For at medisinen som er kapslet inn i nanopartiklene skal være effektiv er det veldig viktig at den når ut til hele svulsten. Derfor trenger nanopartiklene vår hjelp for å nå helt fram. Våre nanopartikler er utviklet her i Trondheim av SINTEF, og de er helt spesielle, fordi de kan danne små bobler. Nanopartiklene legger seg da som et skall rundt overflaten på en boble med gass.
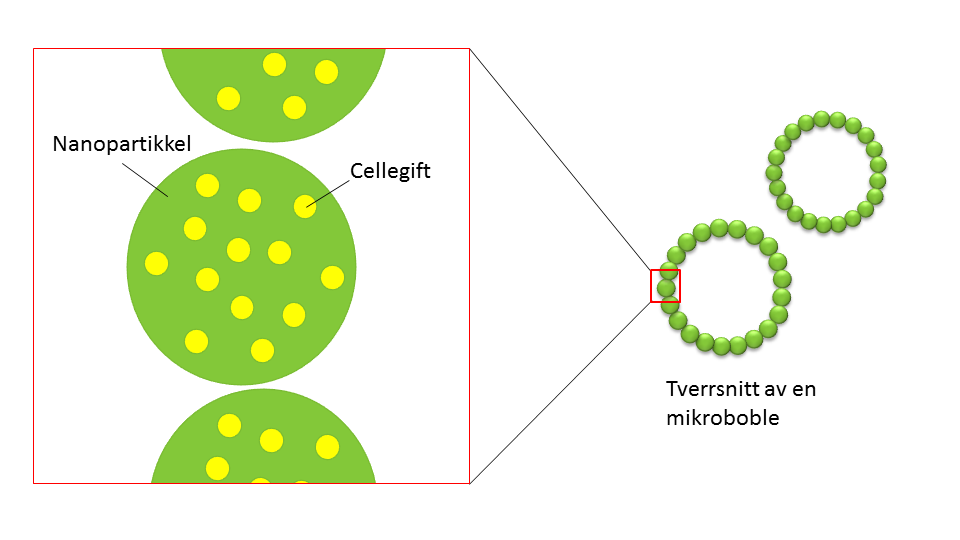
Figur 1: Skjematisk illustrasjon av nanopartiklene som inneholder cellegift, og som danner små mikrobobler med gass. Nanopartiklene er ca 150 nm i diameter, og mikroboblene ca 2 µm.
Disse boblene sprøyter vi inn i blodet og svulsten behandles med ultralyd. Når boblene ankommer svulsten vil ultralydbølgene få boblene til å vibrere og etterhvert sprekke, slik at nanopartiklene løsner og skytes ut fra boblen. Disse vibrasjonene og strømningene vil massere blodårene og vevet, og danne enda flere porer i blodåreveggen. På denne måten dytter vi nanopartiklene ut av blodårene og lenger ut i kreftvevet.
Jeg forsker på hvordan ultralyden påvirker transporten av nanopartikler til svulster i mus. For å få boblene til å oppføre seg som vi ønsker har jeg testet en rekke ulike ultralydbehandlinger med ulikt trykk, og målt hvor mye nanopartikler jeg får levert til kreftvev i mus. Mange av behandlingene har ikke noen effekt, men én behandling ser ut til å fungere veldig bra. Med denne behandlingen får vi levert mer enn dobbelt så mye nanopartikler til svulsten, enn om vi ikke bruker noen ultralyd. Det vil si at hele 250 ganger mer av dosen som går til svulsten, sammenlignet med tradisjonell cellegift alene.
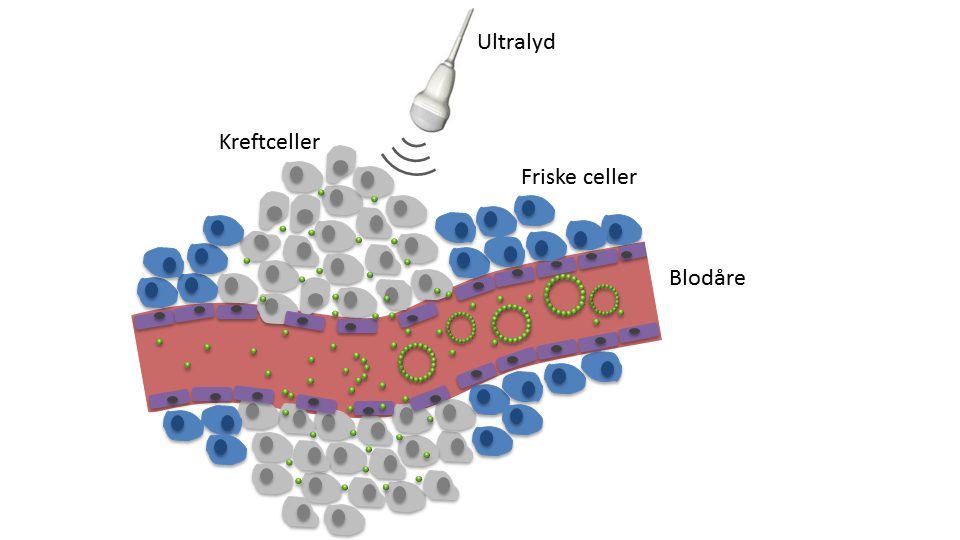
Figur 2: Skjematisk illustrasjon som viser hvordan mikroboblene ankommer svulsten. Der blir de knust av ultralyden slik at nanopartiklene dyttes ut i vevet til kreftcellene. På denne måten kan vi transportere cellegift mer effektivt til kreften, og dermed få mindre bivirkninger av behandlingen.
Etter at boblene har reist gjennom blodårene til svulsten, og levert nanopartiklene ut i vevet og frem til kreftcellene, gjelder det å få cellegiften helt i mål. For at cellegiften skal virke, må den leveres inn i hver enkelt kreftcelle. For å studere denne prosessen dyrker jeg kreftceller i laboratoriet og studerer dem i mikroskop. Det vi ser er at nanopartiklene kamuflerer cellegiften og at kreftcellene spiser nanopartiklene våre med glede. Siste skritt er å få nanopartiklene til å gi fra seg cellegiften, akkurat der og når det trengs. Det er helt nødvendig for å få en effektiv behandling.
Ved å endre den kjemiske sammensetningen til nanopartiklene kan vi skreddersy egenskapene deres. Blant annet kan vi dermed bestemme hvor raskt nanopartiklene skal brytes ned. Etter at nanopartiklene har blitt spist løser de seg opp, slik at cellegiften frigjøres inne i cellen. Da vil kreftcellen slutte å dele seg og etter hvert skrumpe inn og dø.
Kurerer kreft i mus
Basert på disse spennende resultatene har jeg i høst gjennomført den aller første behandlingsstudien. Der ble mus med svulster behandlet med bobler med cellegift og ultralyd 2 uker på rad. Svulster som ikke får noen behandling vokser kontinuerlig i en viss hastighet. Når jeg behandler musene med bobler med cellegift kan veksten reduseres noe, og størrelse på svulstene er stabil over flere uker. Med bruk av ultralyd i tillegg ser vi at veksten stopper opp, svulstene krymper, og musene blir kurert. I likhet med mennesker ser man ofte at mus får bivirkninger fra cellegift, som for eksempel vekttap. Musene i denne studien har ikke tapt noe vekt, og det er veldig lovende.
Også for sykdommer i hjernen
Med dette systemet trenger man ikke å begrense seg til å levere en medisin av gangen. Antagelig kan man også levere kombinasjoner av ulike medisiner, som man vet vil virke godt sammen. I tillegg kan man bruke dette til ulike typer kreft fordi man kan bruke ultralyden lokalt akkurat der det trengs. Det åpner også for et annet spennende bruksområde for våre bobler, nemlig sykdommer i hjernen.
Hjernens blodårenettverk er nemlig ganske så ulikt fra det i svulster. Hjernen er godt beskyttet fra alle stoffer i blodet, og slipper kun inn akkurat det hjernecellene våre trenger. Dette er det som kalles blod-hjerne barrieren. På grunn av den er det svært vanskelig å levere medisin til hjernen, og for mange sykdommer finnes det derfor enda ingen behandling. Men ved bruk av ultralyd og våre bobler har vi vist at vi kan levere nanopartikler over denne barrieren og til hjernecellene. Det kan være veldig spennende for behandling av for eksempel kreft i hjernen, men vi tror også at dette kan gi håp for en skånsom behandling av andre alvorlige sykdommer i hjernen.
Vi fortsetter nå med prekliniske studier, og ønsker å teste dette i større dyr i løpet av de neste årene. Deretter er målet å teste boblene i kliniske studier, slik at de etter hvert kan tas i bruk i klinikken. Prosjektet er et tverrfaglig samarbeid mellom SINTEF, NTNU og Universitetssykehuset St. Olavs hospital. I deler av prosjektet samarbeides det også med Universitet i Bergen og Universitet i Oslo. Prosjektet er finansiert av Helse Midt-Norge og Norges Forskningsråd.

