Bloggere: Trygve Andreassen, Senior ingeniør, og Siver Moestue, Førsteamanuensis
MR Cancer-gruppen, Institutt for sirkulasjon og bildediagnostikk
Forskere over hele verden driver intens jakt på nye måter å drepe kreftceller på. Man leter etter såkalte «drug targets» – altså proteiner som kreftcellene er avhengige av for å kunne dele seg raskt og ukontrollert. I et samarbeid med Karolinska Institutet i Sverige, har vi oppdaget et slikt protein. Det heter CHPT1, og vi tror det kan være mulig å utvikle nye legemidler mot brystkreft basert på denne oppdagelsen.
Nåla i høystakken
Før noen begynner å utvikle et nytt legemiddel mot kreft, må de ha en ide om hva dette legemidlet skal gjøre. Man må identifisere et «drug target» – altså et protein som legemiddelet skal kjenne igjen, binde seg til og endre funksjonen til. Det er ikke så enkelt som det kan høres ut som – vi har omtrent 20.000 forskjellige proteinkodende gener i vårt DNA, og det har blitt anslått at disse kan lage opptil 100.000 forskjellige proteiner (Savage, Nature 2015). Disse proteinene kommuniserer med hverandre på mange forskjellige måter, noe som betyr at vi prøver å finne nåla i en temmelig diger høystakk.
Kreftmedisiner er ofte designet for å blokkere prosesser som er viktige for kreftcellenes deling, eller kopieringen av DNA som skjer i forkant av hver eneste celledeling. I vår forskningsgruppe er vi interessert i kreftcellenes metabolisme (for å vokse og dele seg raskt har kreftceller omprogrammert sitt eget stoffskifte), og vi har derfor lett etter mulige målproteiner i de biokjemiske reaksjonsveiene.
I et samarbeid med Karolinska Institutet i Sverige tok vi utgangspunkt i noen kjente egenskaper hos brystkreftceller: De vokser ofte raskere når de påvirkes av østrogen; og de har unormalt høy omsetning av molekylet kolin. For å studere omsetningen av kolin bruker vi en teknikk som heter MR-spektroskopi.
Hovedmistenkt: CHPT1
Først identifiserte vi ca. 18.000 områder i DNA der østrogen bindes, og fant at disse områdene styrer uttrykket av om lag 2.500 gener. Deretter fant vi ut hvor mange av disse genene som kunne være involvert i omsetning av kolin – og reduserte derved antall kandidatgener til 19. Ved å tolke MR-spektre fra kreftceller dyrket med og uten østrogenstimulering fant vi deretter ut hvilke metabolske endringer østrogen utløser, og kunne dermed redusere antallet proteiner ytterligere – faktisk endte vi opp med å mistenke at proteinet CHPT1 var sterkt involvert i overføring av østrogenets stimulerende effekt til det metabolske maskineriet i kreftcellene.
For å forsikre oss om at dette ikke bare gjelder kreftceller i en laboratorieskål, men også i svulster fra kreftpasienter, undersøkte vi tumorvev fra 70 pasienter med brystkreft. Her fant vi høyere uttrykk av CHPT1 i tumorvev sammenlignet med normalt brystvev. Ekstra interessant var det at svulster klassifisert som østrogenfølsomme hadde betydelig høyere CHPT1-uttrykk enn resten av svulstene. Det tyder på at østrogen faktisk aktiverer CHPT1 også i brystkreftpasienter.
Neste trinn på veien mot å bevise at CHPT1 er et relevant drug target var å se hva som skjer hvis vi slår av dette genet. Det finnes molekylære verktøy som relativt enkelt lar oss stanse produksjonen av CHPT1-proteinet i kreftcellene på laboratoriet, og vi fant ut at kreftcellene vokste mye saktere dersom CHPT1 var slått av (Figur 1).
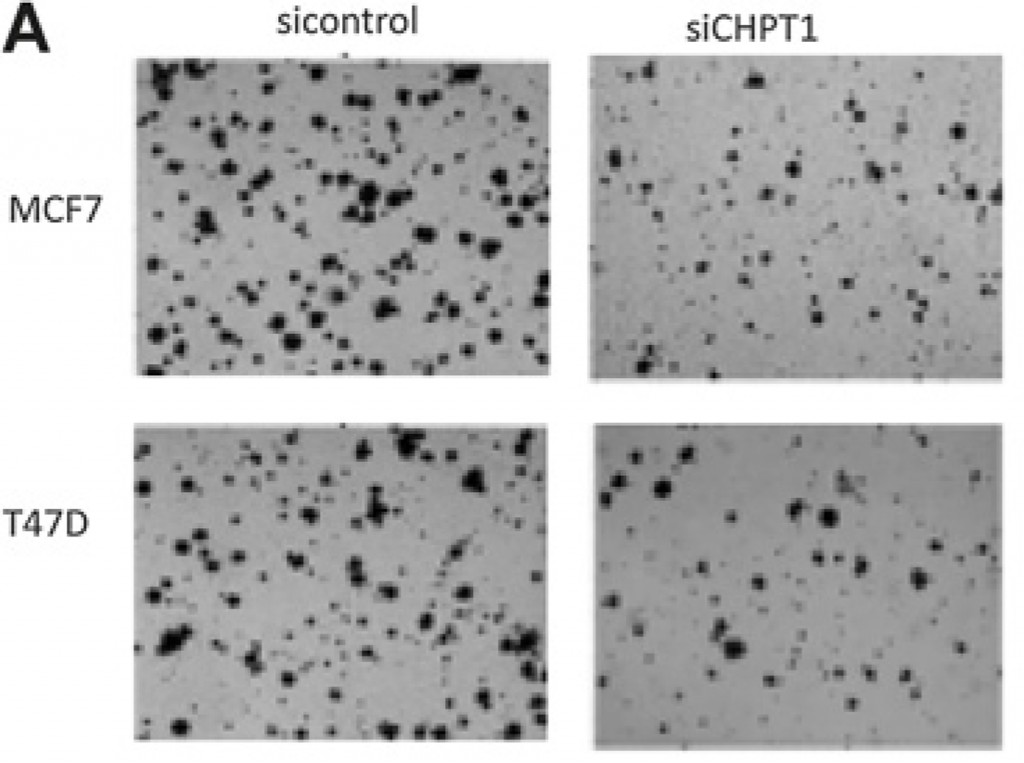
Figur 1: De to bildene til venstre viser to forskjellige typer brystkreftceller, slik de ser ut i mikroskopet når de får vokse fritt i en skål. I bildene til høyre (merket siCHPT1) ser vi de samme cellene, men her har vi «slått av» CHPT1. Det blir tydelig færre celler, noe som tyder på at cellene trenger CHPT1 for å kunne vokse og dele seg.
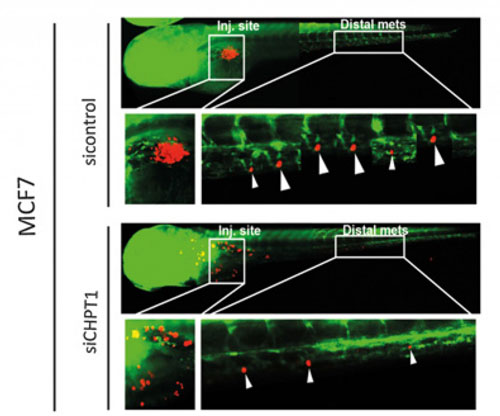
Som kjent er det ingen sak å drepe kreftceller i en skål i laboratoriet, så neste steg var å se om vi kunne påvirke veksten av en tumor i en levende organisme. Av alle ting falt valget på sebrafisk (de er ganske gjennomsiktige, så det er lett å følge med på kreftcellenes skjebne…). Her fant vi at ved å slå av CHPT1 hemmet vi ikke bare tumorveksten, men også kreftcellenes evne til å spre seg til andre vev og organer (Figur 2).
 Alt i alt er dette en temmelig overbevisende rekke med indisier som tyder på at CHPT1 kan være et godt drug target for legemidler til bruk i østrogenfølsom brystkreft. Det er likevel mye vi ikke har funnet ut ennå: Går det an å designe molekyler som blokkerer CHPT1? Hvilke bivirkninger vil de ha? Er de mer effektive enn legemidlene som allerede finnes? Vi har publisert våre funn og håper at noen tar opp hansken og jobber videre med ideene våre, slik at man kanskje får utviklet et nytt legemiddel basert på vår grunnforskning i framtiden.
Alt i alt er dette en temmelig overbevisende rekke med indisier som tyder på at CHPT1 kan være et godt drug target for legemidler til bruk i østrogenfølsom brystkreft. Det er likevel mye vi ikke har funnet ut ennå: Går det an å designe molekyler som blokkerer CHPT1? Hvilke bivirkninger vil de ha? Er de mer effektive enn legemidlene som allerede finnes? Vi har publisert våre funn og håper at noen tar opp hansken og jobber videre med ideene våre, slik at man kanskje får utviklet et nytt legemiddel basert på vår grunnforskning i framtiden.
Prosjektet er gjennomført med støtte fra Kreftforeningen og Forskningsrådet.

